LES MOLECULES ET LES
IONS
Les ions
Définition
Un ion est un atome (ou groupe d’atomes), ayant perdu (ou gagné) un (ou plusieurs) électrons.
· Un atome qui a perdu un ou plusieurs électrons est un ion positif ou cation.
Exemples: Na+; K+; Ca2+
· Un atome qui a gagné un ou plusieurs électrons est un ion négatif ou anion.
Exemples Cl-; I-;
O2-
Ions monoatomiques
Ils sont constitués d’un seul atome.
Exemples:H+; Cl; Al3+
Les ions monoatomiques sont, comme les
atomes, des représentants des éléments.
Ions polyatomiques
Il existe des ions
formés des ions à partir de plusieurs atomes. Ils sont des ions polyatomiques.
Exemple: H3O+;
SO42-
Remarques:
Les éléments dont les atomes ont
tendance à perdre des électrons pour devenir des ions positifs sont dits électropositifs.
Les éléments dont les atomes ont
tendance à gagner des électrons pour devenir des ions négatifs sont dits électronégatifs.
Les molécules
Définition
Une molécule
est un assemblage, électriquement neutre, formé des atomes liés entre eux.
Une molécule peut être monoatomique
(formée d’un seul type d’atome).
Exemples: H2; O2
Une molécule peut être polyatomique (formée
de plusieurs types d’atomes).
Exemples: H2; NH3
La liaison entre deux atomes d’une
molécule est appelée liaison covalente.
L’atomicité d’une molécule est le
nombre d’atomes qu’elle contient.
Représentation d’une molécule
- La formule
brute d’une molécule est obtenue par juxtaposition des symboles des
éléments constituant cette molécule. Chaque symbole porte en indice, en
bas et à droite, le nombre d’atomes de cet élément dans la molécule. Le
nombre 1 n’est pas porté.
Exemple:
H2O: cette
molécule d’eau est constituée de 2 atomes d’hydrogène(H) et 1 atome
d’oxygène(O) ;
HCl: cette molécule d’acide chlorhydrique
(ou chlorure d’hydrogène) est constituée de 1 atome d’hydrogène(H) et 1 atome
de Chlore (Cl);
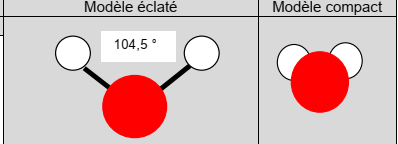
- Une molécule
peut aussi être représentée par des modèles moléculaires.
Les atomes sont modélisés
par des billes dont la couleur est associée à un élément chimique.
Étant donné que la plupart des molécules complexes sont organiques, il a été
choisi d’attribuer
une couleur aux principaux éléments de ce type de substance, à savoir au
carbone, à l’hydrogène,
à l’oxygène, à l’azote, au chlore et au soufre. Par convention, les couleurs
sont les suivantes
:

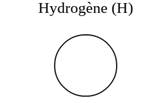
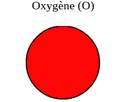
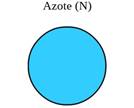
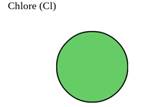

Exemple de la molécule d’eau :
EXERCICES
EXERCICE I:
Recopie et complète les
phrases suivantes:
1. Une ……………….est
un assemblage bien ordonné d’atomes liés entre eux.
2. Lorsqu’une molécule
est constituée d’un seul type d’atomes, c’est une molécule ……………
3. La liaison entre
deux atomes d’une molécule est appelée liaison ……………….
4. La…………….d’une
molécule s’écrit en utilisant les symboles des atomes qui la constituent avec
en indice le nombre de chaque atome.
5. Une molécule peut
aussi être représentée par des………………..
EXERCICE II:
Recopie et complète les phrases suivantes :
1. Un…………………..est
un atome ou un………………d’atomes ayant gagné ou perdu un ou plusieurs électrons.
2. Un……………..est
un ion négatif c.-à-d. un atome ou une molécule ayant………………..au
moins un ………………..
3. Un cation est un ion
……………c.-à-d. un atome ou une molécule ayant………………..au
moins un ……………………
4. Lorsqu’un atome
simple a perdu ou gagné un ou plusieurs électrons, c’est un ion……………..
5. Lorsqu’un groupe
d’atome a perdu ou gagné un ou plusieurs électrons, c’est un ion……………..
EXERCICE III:
Ecris les formules des
corps suivants :
Dioxyde de carbone, eau,
dioxygène, dihydrogène, dioxyde de soufre, Aluminium, Ozone, Monoxyde de
carbone.
EXERCICE IV :
1. Quels sont les ions
issus des atomes ou groupe d’atomes suivants: Cu, Al,
Cl, OH, Mg, SO4
2. Complete le tableau
suivant :
|
Nom de l’ion |
Symbole de l’ion |
Nature de l’ion |
Type d’ions |
|
………… |
Ca2+ |
…………. |
…………. |
|
Ion sulfate |
|
Cation |
|
|
Ion aluminium |
…………. |
…………. |
Monoatomique |
|
|
H3O+ |
……….. |
…………. |
|
Ion chlorure |
…………. |
anion |
………….. |
|
Ion hydroxyde |
………… |
…………. |
Polyatomique |
Avez-vous un exercice à proposer au Forum?Cliquez-ici
Merci de votre visite
Laissez un
commentaire