CLASSIFICATION PERIODIQUE DES ELEMENTS
Notion d’élément chimique
Tous les corps sont constitués d’éléments chimiques. Il existe 118 éléments chimiques connus dont 3 sont en attente de confirmation, 25 artificiels et 93 naturels, à partir desquels sont constitués tous les corps existants. La combinaison des éléments chimiques peut donner une infinité de corps différents.
Définition
L’élément chimique est un corps commun à plusieurs autres corps.
Exemple:
· Le carbone est commun au pétrole, butane, alcool, bougie,
·Le cuivre est commun au métal cuivre, à l’oxyde de cuivre II et à l’ion cuivre.
Symboles des éléments chimiques
Les éléments sont représentés par des symboles. Le symbole d’un élément est toujours une lettre majuscule, la première du nom français ou étranger, suivie quelquefois d’une seconde lettre minuscule pour différenciation.
Exemples:
|
Nom de l’élément |
Symbole de l’élément |
|
Carbone Hydrogène Fer Cuivre Azote Chlore Soufre |
C H Fe Cu N Cl S |
Classification périodique des éléments
Tous les éléments sont groupés dans un tableau qui est le tableau de classification périodique des éléments.
Principe de classification:
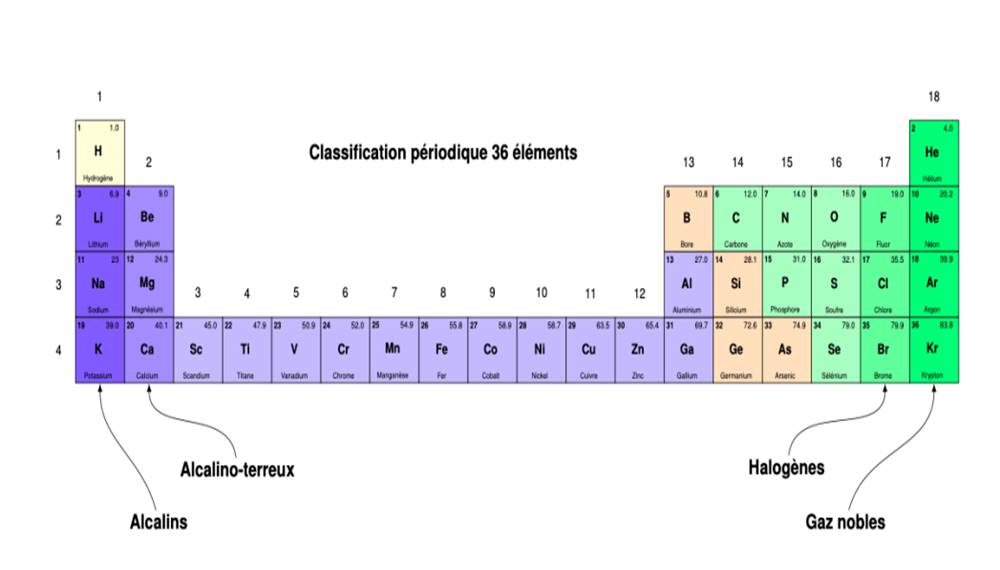
Les éléments, représentés par leurs symboles, sont classés par ordre de numéro atomique croissant dans un tableau à 18 colonnes ou groupes et 7 lignes ou périodes. Chaque élément occupe une case du tableau. Son numéro atomique est situé en haut et à gauche de la case.
Chaque période correspond au remplissage d’une couche électronique. Ainsi, la première période correspond au remplissage de la couche K, la seconde celle de la couche L…Lorsqu’une couche est remplie, on passe à la période suivante, de sorte que tous les éléments d’une même colonne possèdent le même nombre d’électrons périphériques.
Exemples:
-Le groupe de la colonne I est le groupe des alcalins: les atomes de ces éléments possèdent un électron périphérique. A l’exception de l’hydrogène, ce sont les alcalins (lithium, sodium, potassium…)
-Le groupe de la colonne 17 est le groupe des allogènes: les atomes de ces éléments ont 7 électrons périphériques (fluor, chlore, brome, iode…)
-Le groupe de la colonne 18 est le groupe des gaz rares: les gaz rares ou gaz nobles n’interviennent pas dans les réactions chimiques car leur couche externe est saturée mis à part l’hélium. On dit qu’ils possèdent une grande inertie chimique (hélium, néon, argon, krypton).
Différentes familles d’éléments.
a. Les
alcalins.
Première colonne de la classification, ils possèdent tous un seul électron sur
la couche externe.
Ils ont tendance à facilement perdre cet électron (en vertu de la règle de
l’octet) et devenir des cations avec une charge positive.
A l’exception de l’hydrogène, les éléments de la première colonne appartiennent
à la famille des alcalins. Dans la nature on les rencontre sous forme d’ions Li+
(ion lithium), Na+ (ion sodium) ou K+ (ion potassium),
comme dans l’eau ou les eaux minérales. Ils sont responsables du goût salé. A
l’état de corps purs simples ce sont des métaux mous qui réagissent
spontanément avec le dioxygène de l’air ou l’eau.
b. Les alcalino-terreux.
Deuxième colonne
de la classification, ils possèdent deux électrons sur la couche externe,
électrons qu’ils ont facilement tendance à perdre pour donner des cations avec
deux charges positives.
c. Les halogènes.
Dans la 17ème
colonne, ils possèdent sept électrons sur la dernière couche. Ils ont
tendance à gagner un électron pour donner un anion avec une charge négative.
Les éléments de la 17ème colonne (7ème colonne de la classification simplifiée)
appartiennent à la famille des halogènes.
Dans la nature, on les rencontre sous forme d’ions monoatomiques : F-
(ion fluorure) ; Cl- (ion chlorure) ; Br- (ion bromure).
Ils peuvent également exister sous forme de molécules diatomiques : F2
, Cl2, Br2 .
Ces espèces chimiques sont fortement colorées et très nocives.
d.
Les gaz nobles.
Appartenant à la dernière colonne, ils possèdent déjà huit électrons sur la
couche externe : ils sont donc naturellement stables.
Les gaz rares sont peu présents dans l’atmosphère terrestre. Ce sont les
éléments chimiques les plus stables. Ils sont inertes chimiquement c’est-à-dire
qu’ils ne participent à aucune réaction chimique. Ils ne forment pas d’ions ni
de molécules.
L’hélium est l’élément le plus abondant dans l’Univers après l’hydrogène.
Intérêt de la classification périodique des éléments Intérêt de de la classification
· Elle fournit des renseignements importants sur chaque élément chimique:
-son symbole X
-son numéro atomique Z
-sa masse atomique.
· Les atomes des éléments d’une même colonne ont, le même nombre d’électrons périphériques. Ils ont les propriétés chimiques semblables et forment un groupe ou famille.

Numéro atomique Z =8
Masse atomique=16
EXERCICES
EXERCICE I:
p;
En vue d’identifier les éléments chimiques contenus dans le saccharose (sucre),
on fait chauffer du sucre en vase clos.
À l’issu
du chauffage, il se forme du « charbon de sucre » et de la vapeur d’eau.
On demande
d’interpréter ces résultats.
1) Définis
l’élément chimique.
2) Nomme les
éléments chimiques contenus dans le charbon et dans la vapeur d’eau.
3) Déduis
des produits de la réaction chimique, les éléments chimiques contenus dans le
saccharose.
EXERCICE II: Complète le tableau suivant à l’aide des renseignements que tu retrouveras dans la case occupée par chacun des éléments:
|
Nom de l’élément |
Carbone |
Azote |
Chlore |
|
Calcium |
|
|
Symbole |
C |
Cl |
Ca |
|||
|
Numéro atomique (Z) |
2 |
13 |
||||
|
Masse molaire atomique (g.mol-1) |
14.0 |
EXERCICE III: L’élément sodium a pour numéro atomique Z=11
A partir du tableau de classification périodique des éléments, réponds aux questions suivantes:
1. Quel est son symbole?
2. Situe-le dans le tableau de classification simplifié.
3. Quels sont le numéro atomique, le nom, le symbole et la situation dans le tableau simplifié de:
a) L’élément situé directement au-dessus de sa case?
b) L’élément situé directement en-dessous de sa case?
c) L’élément situé à deux cases avant la sienne ?
d) L’élément qui le suit dans le tableau?
4. Quelle est la masse molaire atomique de l’élément sodium.
EXERCICE IV:
Soient
les atomes suivants : C(Z=6), P(Z=15), O(Z=16),Cl(Z=17), F(Z=9).
Donner la localisation de ces éléments dans le tableau périodique (indiquer le
groupe et la période), précisez les électrons de valence, ainsi que le nombre
d’électrons célibataires.
Avez-vous
un exercice à proposer au Forum ?
Cliquez-ici
Merci de votre visite
Laissez un commentaire