NOYAU ATOMIQUE
Les constituants du noyau atomique
Le noyau est constitué des protons et des neutrons. On les appelle des nucléons.
Le proton est chargé d’électricité positive.
Charge du proton: qp=e=1,6.10-19C
Masse du proton: mp=1,67.10-27kg
Le neutron est électriquement neutre, il ne porte pas de charge électrique.
Charge du neutron: qn=0
Masse du neutron : mn=1,67.10-27kg
Les protons sont les seuls responsables de la charge positive du noyau.
Le nombre de charge, appelé numéro atomique Z est égal au nombre de protons contenus dans le noyau.
Le nombre de masse A est égal au nombre de nucléons (protons + neutrons) contenus dans le noyau.
Le nombre de neutrons N est évidement égal à la différence entre A et Z: N=A-Z
Représentation d’un noyau atomique
![]()
Isotopes
Les atomes qui ont le même numéro atomique Z, mais de nombre de masse A différents, sont des isotopes de l’élément de numéro atomique Z.
Exemple: ![]() et
et ![]() sont les isotopes de
l’uranium
sont les isotopes de
l’uranium
Nucléides
On appelle nucléide, une espèce atomique caractérisée par le nombre de protons et de neutrons dans son noyau, ainsi que par son état énergétique.
Ainsi, les isotopes sont des nucléides qui ont le même nombre de protons (numéro atomique Z) mais un nombre de neutrons différent.
Aspect énergétique des noyaux
Défaut de masse
Le défaut de masse d’un noyau de
symbole ![]() est la différence entre
la masse des nucléons isolés et au repos et la masse du noyau au repos. On le
symbolise par:
est la différence entre
la masse des nucléons isolés et au repos et la masse du noyau au repos. On le
symbolise par:
![]()
Les masses sont exprimées en unité de masse atomique (symbole u).
1u =1,66054.10-27 Kg
Le défaut de masse est toujours positif.
Equivalence Masse-Energie (Relation de d’Einstein)
Toute particule, même au repos, possède, du simple fait de sa masse, une énergie E0 appelée énergie de masse et dont la valeur est donnée par la relation:
E0=mc2
m en kilogramme (kg)
c en mètre par seconde(ms-1)
E0 en joules(J)
Dans cette relation, on prend:
c =3.108 m/s.
En physique nucléaire, l'unité convenable de l'énergie est l’électronvolt et un de ses multiples comme mégaélectronvolt MeV
![]()
![]()
Energie équivalente à l'unité de masse atomique :
D’après la relation d’Einstein et pour la masse égale à 1 u, on a:
E=mC2=1,66054.10-27x299792458)2=1492,41.10-13 J
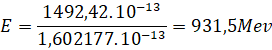
![]()
Energie de liaison
L’énergie de liaison E#8467; d’un noyau atomique est l'énergie qu'il faut fournir au noyau au repos pour le dissocier en ses nucléons constitutifs pris au repos. (E#8467; est une grandeur positive.).
![]()
On l’exprime par la relation:
![]()
![]()
Cette énergie est positive.
Elle s’exprime en mégaélectronvolt (MeV):
Energie de liaison par nucléon
L'énergie de liaison par nucléon est définie par la relation :
![]()
Son unité est le MeV/nucléon.
A partir de l’énergie de liaison par nucléon, on peut comparer la stabilité de 2 noyaux radioactifs : Plus l'énergie de liaison par nucléon est grande plus le noyau est stable.
EXERCICES
EXERCICE I:
1.Calculer
en Mev l’énergie de liaison du noyau de Lithium ![]() .
.
![]()
On
donne: mp=1,0073 u; mN=1,0087 u; m (![]() )=7,0160 et u=1,66.10-27
kg.
)=7,0160 et u=1,66.10-27
kg.
2. Calculer, en Mev/nucléon, l’énergie de liaison par nucléon
du noyau du Lithium ![]() .
.
3. Calculer l’énergie libérée au cours de la transformation ci-dessous:
![]()
On donne :
m(S) = 5,30763.10-26kg; m(P) = 5,30803.10-26kg; m(e) = 9,1.10-31kg.
EXERCICE II:
On considère la réaction classique de fusion entre un noyau de Deutérium et un noyau de tritium:
![]()
Déterminer l’énergie libérée au cours de cette transformation.
Données:
|
|
Hélium |
Tritium |
Deutérium |
Neutron |
|
Masse en u |
4,0015 |
3,0247 |
2,0160 |
1,0087 |
Unité de masse atomique: 1u =1,66054.10-27 Kg
Célérité de la lumière: c =3.108 m/s.
Méga-électron-volt: ![]()
Avez-vous un exercice à proposer
au Forum?Cliquez-ici
Merci de votre visite
Laissez un commentaire